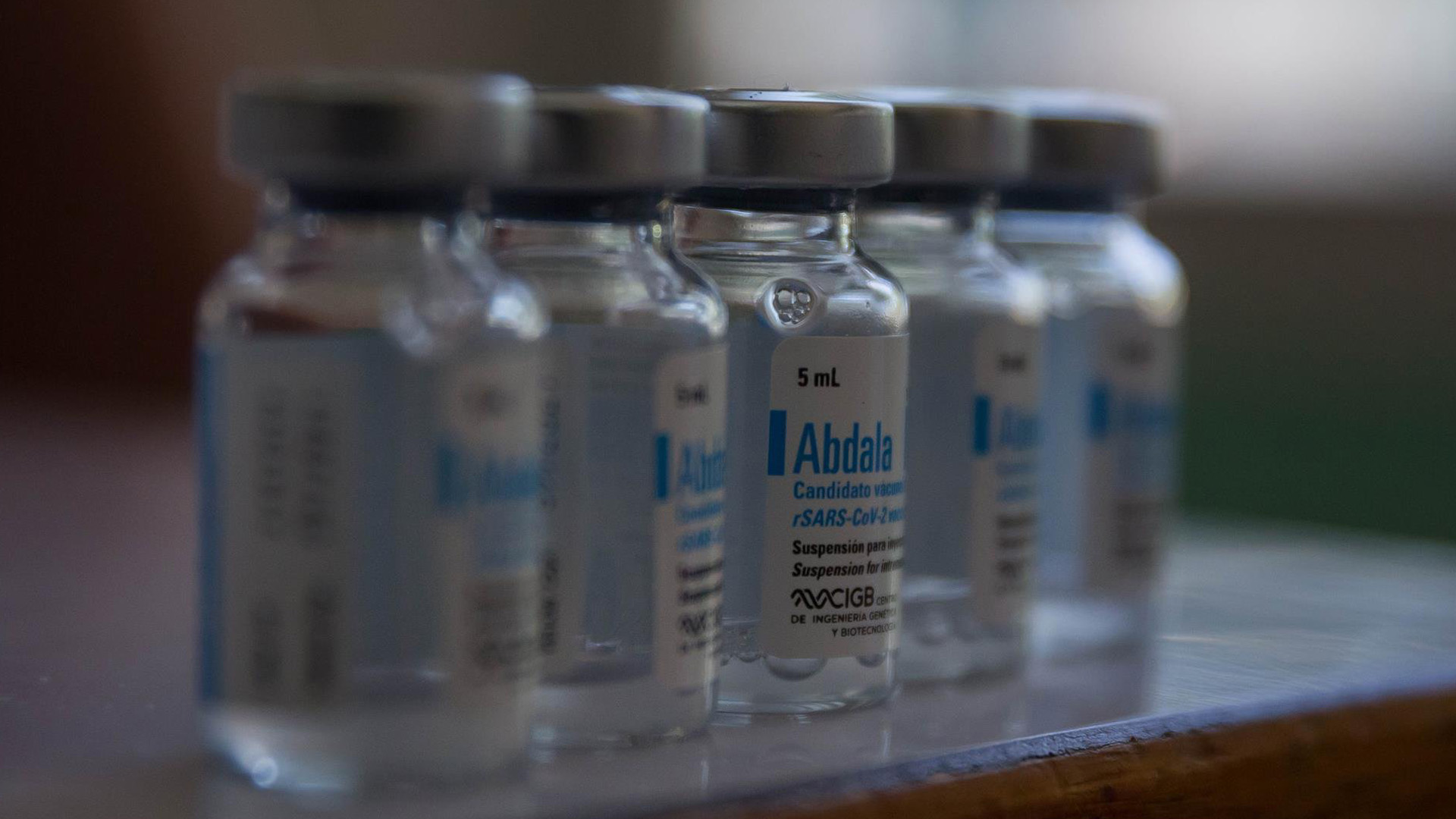
Alertan que la aplicación del prototipo cubano de vacuna en Venezuela está repleta de irregularidades, violación a derecho a la información y a la salud y a procedimientos nacionales e internacionales de investigación científica
Foto: @ENCiudadanoCCS/Archivo
El Centro Nacional de Bioética (CENABI) difundió este 20 de julio un comunicado en el que expresa su rechazo a la aplicación experimental del candidato a vacuna contra el Sars-Cov2 “Abdala” en Venezuela.
En el texto, el grupo de expertos alertó que la vacunación en el país con Abdala no cumple con las normas éticas que regulan la investigación en seres humanos. Refieren que dos días antes del anuncio del Estado venezolano de que iba a adquirir doce millones de dosis de este producto experimental alertaron que el candidato no había sido aprobado por los organismos internacionales pertinentes.
Además, ratifican que la eficacia e inocuidad del prototipo de vacuna no han sido demostradas.
“Lejos de reconsiderar esta decisión, la Misión Médica Cubana inició en la última semana de junio la aplicación de 10.000 dosis del producto, en el complejo urbanístico Ciudad Tiuna, a comunidades de bajos recursos y mayor control estatal, a las cuales no se les informó que estaba participando en una investigación”, añaden.
Indican también que Abdala se está usando para inmunizar en Venezuela antes de que se concluyan los ensayos en fase 3 del Centro de Ingeniería Genética y Biotecnología (CIGB) cubano, -el cual estima que sus resultados estarán disponibles para el 16 de agosto- y antes de tener la autorización de uso de emergencia por el organismo supervisor de ese país, el Centro Estatal Cubano de Medicamentos (Cecmed), la cual fue emitida prematuramente el 09-07-21.
La fase 3 es una etapa crucial en el proceso de desarrollo de cualquier fármaco. En el caso de las vacunas, es la prueba de fuego que mide su eficacia, es decir, si protegerá o no contra la infección . La fase I evalúa inocuidad o efectos adversos, y en la fase II se estudia la inmunogenicidad, es decir, si la candidata ayudó a producir anticuerpos contra el virus.
“Más irregular aún resulta la autorización de uso en emergencia en Venezuela, que precedió en 8 días a la del país fabricante”, señalan.
Las violaciones a derechos y pasos científicos detectadas por el Centro Nacional de Bioética
El Centro Nacional de Bioética también hace énfasis en los rigores científicos y derechos que se han vulnerado durante proceso de aplicación de Abdala en Venezuela.
“Se ha faltado a la verdad y se viola el derecho a la información. Las personas acuden bajo engaño, creyendo que se les va a aplicar una vacuna efectiva; no se les dice que
participan en un ensayo clínico. Esto puede hacer que se sientan seguras y disminuyan las medidas de protección. El programa recibe la denominación de ‘Intervención sanitaria’ y ¡Jornada Territorial de vacunación’, no de estudio, como lo lo califica el representante en Venezuela de la biofarmacéutica estatal cubana BioCubaFarma y los envases del producto están rotulados como ‘Candidato a vacuna’”, detallan.
Otro punto importante que señalan como falta es que, en los avisos de convocatoria, se afirma que el producto cuenta con la aprobación de la OMS, lo que ha sido
desmentido por los organismos sanitarios internacionales.
Además, se le atribuye una eficacia mayor del 92%, cuando aún no se ha concluido el estudio.
De igual forma, señalan que se han violado normas que rigen la investigación en seres humanos, tanto las nacionales (contempladas en el Código de Ética para la Vida, Reglamento de Investigación en Farmacología Clínica del Instituto Nacional de Higiene Rafael Rangel y capítulos de la Ley de Ejercicio de la Medicina y del Código de Deontología Médica) como las internacionales ( especificadas en el Código de Nüremberg, Declaración de Helsinki, Pautas CIOMS/OMS, Guía ICH de Buenas Prácticas Clínicas).
Al respecto, citan las más evidentes violaciones encontradas:
1-. Ausencia de un protocolo de investigación formal, aprobado previamente por el Comité de Ética del organismo asistencial donde se realizará el estudio y por el Instituto Nacional de Higiene Rafael Rangel.
2-. Documento impreso para la obtención del consentimiento informado que respete la autonomía del participante y la justicia para la población en estudio. Este consentimiento debe ser aprobado previamente por el Comité de Bioética, debe contener una 1ª parte con información sobre la naturaleza experimental de los procedimientos, objetivos del estudio, descripción del producto a recibir, de los resultados de investigaciones previas y de todos los procedimientos a los que va a ser sometido el sujeto y con cuyo cumplimiento se está comprometiendo, beneficios esperados para la persona, la población y/o el conocimiento científico, razón por la que la persona se ha incluido en el estudio, riesgos y complicaciones a los que se somete y su frecuencia estimada, responsabilidad de los investigadores ante las mismas (a quién acudir, cómo y dónde hacerlo, cobertura por pólizas de seguro), compromiso de confidencialidad en el manejo de la información suministrada y libertad para negarse a participar o
retirarse luego de haber aceptado sin ser objeto de sanción.
En la 2ª parte del documento, el participante o su representante legal deben hacen constar que han entendido la información y aclarado sus dudas satisfactoriamente, que están conscientes de los compromisos adquiridos por ellos y por el investigador y que aceptan libremente participar.
Finalmente, este “contrato” debe ser firmado por el sujeto o su representante legal, el investigador principal y uno o dos testigos. Se ha conocido de un documento de consentimiento informado que se ha hecho firmar a algunos participantes, pero este no cumple con estos requisitos y no ha sido aplicado cuando corresponde: previo a la primera aplicación, sino con motivo de la segunda.
3-. Los estudios de prototipos vacunales requieren la comparación de las personas que reciben el producto, con un número equivalente de las mismas que reciben un placebo (producto inerte). Si existe rigurosidad científica en este estudio y se esta administrando placebo sin informarlo en el consentimiento, hay un fraude adicional a las personas que lo reciben, asumiendo que se trata del producto prometido.
4-. No se tiene evidencias de la competencia del equipo investigador, no se conoce su trayectoria en investigación e, incluso, sus credenciales como profesionales de la medicina; en consecuencia, el seguimiento de los participantes, indispensable para detectar y tratar efectos indeseables (Principio de No Maleficencia) y valorar la eficacia del producto (Principio de Beneficencia), no están asegurados.
Reprueban aplicación en menores
El Centro Nacional de Bioética ve con especial preocupación el anuncio de la aplicación del candidato vacunal Abdala en niños y adolescentes.
“Esto reviste una gravedad mayor, tratándose de poblaciones especialmente vulnerables, debido a sus procesos biológicos particulares y
a sus limitaciones para consentir libremente. Solo se permiten investigaciones en menores de edad cuando estas responden a sus problemas particulares y la eficacia e inocuidad de los productos biológicos ha sido comprobada en adultos, advierten”.
La semana pasada, un grupo de docentes y enfermeras protestó contra esta posibilidad y manifestaron que los niños y adolescentes del país “no deben se tratados como conejillos de indias”. Los reclamos sobre este tema han sido constantes a través de las redes sociales.
#16Jul #Coronavirus #Venezuela
Ana Rosario Contreras, presidenta del Colegio de Enfermeras de Caracas, pide vacunar al 70% de los adultos en Venezuela para que sea seguro el retorno a clases en el país – @vivoplaynetpic.twitter.com/fPcqvD9xkN— Reporte Ya (@ReporteYa) July 16, 2021
Al grito de “más claro y más sencillo, los venezolanos no somos conejillos”, mujeres integrantes del Frente Amplio junto a un grupo de enfermeras protestaron frente a la sede del PNUD para exigir vacunas y rechazar la posible aplicación del candidato Abdala a niños –@GabyGabyGG pic.twitter.com/cSxsoWCWz1
— El Pitazo (@ElPitazoTV) July 16, 2021
Cómo madre me preocupa q nuestros hijos sean utilizados como conejillos de Indias!! Abdala no es una vacuna. Es un producto biológico experimental que no ha sido autorizado por el Centro de Control de Medicamentos Cubanos ni la OPS. pic.twitter.com/yJuxCOCKIr
— Karin Salanova (@karinsalanova) July 15, 2021
Concejal Kadary Rondon: desde el #PNUD rechazamos el experimento cubano Abdala, nos negamos a que nuestros hijos sean conejillos de indias.#ConMisHijosNo @EnCiudadanoCcs pic.twitter.com/VbxksOlHnh
— Radio Caracas Radio (@RCR750) July 17, 2021
Por último, el Cenabi alerta que esta situación empeora la ya grave situación de la pandemia de COVID 19 en el país, y hacen sus votos porque se garanticen “vacunas eficaces, seguras, de aplicación más sencilla y de menor costo que este prototipo, que logren proteger de las formas más graves de la enfermedad, disminuir los contagios y que limiten aparición de nuevos mutantes”.
“Mientras esto no sucede, se sigue violando el derecho a la vida y a la salud de los venezolanos”, concluyen.
Con información de Nota de Prensa